Qu'est-ce que le syndrome de Wolff-Parkinson-White ?
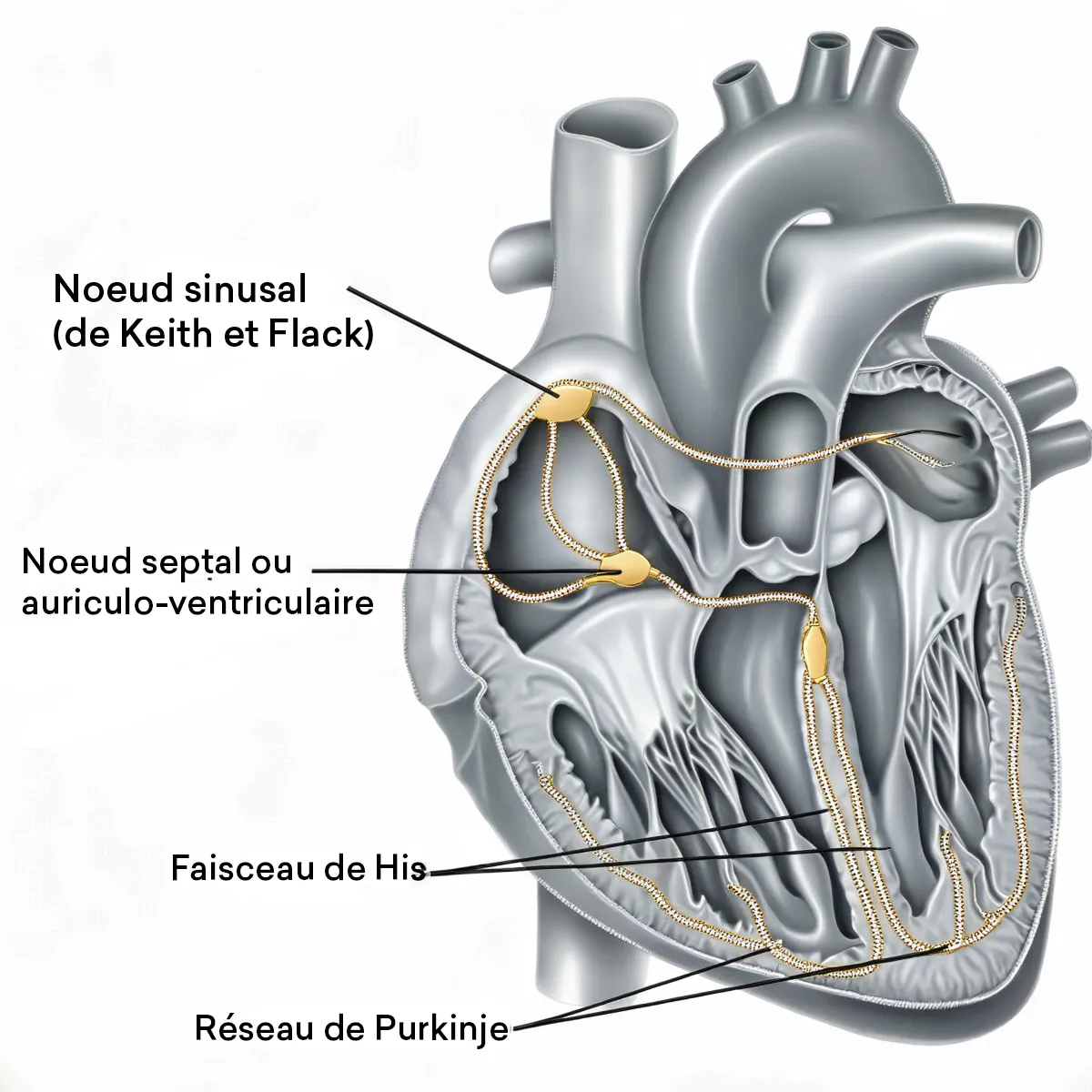
Le syndrome de Wolff-Parkinson-White est une anomalie congénitale du système électrique du cœur. Il se caractérise par la présence d’une voie de conduction supplémentaire, appelée faisceau accessoire ou faisceau de Kent, qui relie directement les oreillettes aux ventricules.
Cette condition est à l’origine d’un type particulier de tachycardie supraventriculaire : la tachycardie jonctionnelle par réentrée sur faisceau accessoire. Cette forme d’arythmie est parfois aussi appelée « maladie de Bouveret », du nom du médecin français qui en a décrit les manifestations cliniques à la fin du 19ème siècle, bien avant que son mécanisme électrophysiologique ne soit compris.
Le syndrome de Wolff-Parkinson-White concerne environ 1 à 3 personnes sur 1000 dans la population générale. Il peut être diagnostiqué à tout âge, mais les premiers symptômes apparaissent souvent entre l’adolescence et le début de l’âge adulte.